
Cas9 通常很擅长 基因 昏死。 除非它不是。 大多数被弄湿的人 基因编辑 在下面的凝胶中有过类似的经历,其中一些指南工作得很好,但其他人则是绝对的狗。
如果您有定位限制(例如 在追求功能域时 而不是只是随机放置切割)。 那么我们能做些什么呢?
TL博士 在使用 Cas9 RNP 时添加非同源单链 DNA 极大地促进了基因敲除。
该问题
已经有 一些 很不错 显示 Cas9 更喜欢某些指南的论文。 我将这些称为 One True Guide 假设,其想法是 Cas9 以某种方式进化为喜欢某些原始空间而不喜欢其他人。 数据不会说谎,这确实是事实——Cas9 喜欢 G 靠近 PAM 并且讨厌使用 C。但是指南是 在一种细胞系中高度活跃在其他细胞系中很差,并在小鼠中比较非常偏爱的实验 细胞 vs 蠕虫给出了截然不同的答案。 如果问题仅在于 Cas9 使用 向导RNA 切开。
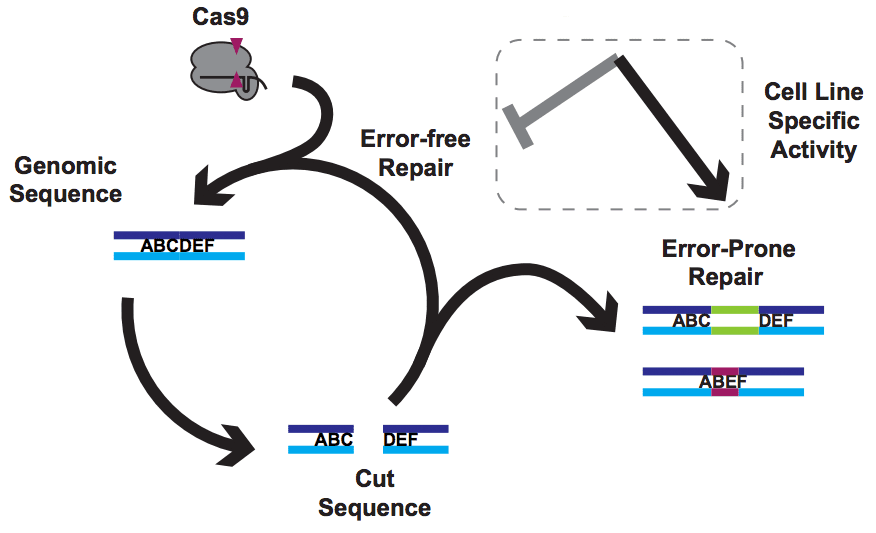
但当然,Cas9 只是在削减。 其他一切都归结为 的DNA 由宿主细胞修复。
我们的方案
在我实验室的一篇新论文中, 刚刚在自然通讯中,我们发现使用简单的技巧搞乱 DNA 修复可以挽救完全不活动的指南,并使分离敲除克隆变得容易,即使在具有挑战性的(例如多倍体)环境中也是如此。 我们称这种方法为“NOE”,即非同源寡核苷酸增强。
(这个首字母缩略词对我来说实际上是一个私人笑话,因为我曾经在 一个非常不同的背景及 诺谷 是旧金山的一个不错的小社区)
如何执行 NOE? 其实超级简单。 使用 Cas9 时 核糖核酸 对于编辑,只需将非同源单链 DNA 添加到您的电穿孔反应中。 就是这样。 这增加 插入 频率在各种细胞系中的数倍,即使使用通常表现不佳的指南也很容易找到纯合敲除。
NOE 的关键是拥有额外的 DNA 末端。 单链 DNA 效果最好,甚至同源 ssDNA 也可能用于 HDR 工作。 我们倾向于使用与人类不同源的 ssDNA 基因组 (例如来自 BFP 的一些序列)因为它们使编辑结果更简单(NHEJ 仅代替 NHEJ + HDR)。 但双链 DNA 也有效,甚至剪过的鲑鱼精子 DNA 也能奏效! 质粒 都不好,因为没有自由的目的。
我们知道 NOE 正在对 DNA 修复起作用,因为虽然这在许多细胞系中起作用,但细胞之间的分子结果不同! 在许多细胞(我们测试过的 5/7)中,NOE 会导致出现非常大的缺失(比使用 Cas9 时通常看到的要大得多)。 但是在测试的 2/7 细胞中,NOE 反而导致细胞开始清除双链 DNA 的小片段并将它们放入 Cas9 断裂处! 这些 DNA 片段的连接点看起来像微同源性,但我们还没有做过遗传实验来说明这是由微同源性介导的末端连接等过程引起的。
这里发生了什么?
对 DNA 修复的改变如何如此显着地影响给定指南的明显功效? 我们认为我们的数据以及来自其他实验室的数据意味着 Cas9 切割频繁发生 完美 修复。 但这引入了一个徒劳的循环,其中 Cas9 重新绑定和重新切割同一个站点。 我们观察编辑的唯一方法是当这个循环通过不完善的修复退出时,导致插入。 完美修复对于正常的 DNA 处理很有意义,因为我们在正常生活中一直在积累 DNA 损伤。 如果这种损坏经常导致插入缺失,我们确实会感到抱歉。 似乎 NOE 要么抑制完美修复(例如滴定出 Ku?)或增强不完美修复(例如刺激 ATM 响应?),尽管我们目前仍然缺乏有关机制的直接数据。

到底有什么好处呢?
刺激双链 DNA 掺入断裂的能力可能是有用的,因为双链盒的非同源或微同源介导的整合最近已用于 基因标记. 但是我们还没有明确地尝试过这个。 我们还发现 NOE 对于阵列筛选非常有用,其中编辑效率是表型外显率和后续命中调用的关键。
重要的是,NOE 似乎在原代细胞中起作用,包括造血细胞 干细胞 和 T细胞. 我们在无法培养的原代人类细胞中进行合并编辑时一直使用它,并发现在使用 NOE 时,更高比例的细胞具有基因破坏。 到目前为止,我们只使用 RNP 在人体细胞中工作过,我很想听听人们在其他生物体中使用 NOE 的经验。 我们没有太多运气尝试使用基于质粒的 表达 Cas9,但其他团队告诉我,他们也可以让它在这种情况下工作。
我该如何尝试?
所以如果你有兴趣,不妨试一试。 详情都在我们最近的 自然通讯论文,但如果您有任何其他问题,请随时与我们联系。 这项工作是由 Chris Richardson(为您带来 翻板退火 HDR 捐助者),Jordan Ray(杰出的本科生,现在是麻省理工学院的研究生),以及 缺口 Bray(博士后生物信息学专家)。


