
消息
发现 CRISPR“剪切和粘贴”中的隐藏步骤
IGI | 玛雅·科斯特曼 | 27 年 2018 月 XNUMX 日
CRISPR切割后的DNA修复与人们想象的完全不同
伯克利新闻 | 罗伯特·桑德斯 | 30 年 2018 月 XNUMX 日
尽管寄予厚望和大量投资 CRISPR-Cas9 基因编辑,科学家们仍然有很多东西要了解它是如何在人类中发挥作用的。
在最新的例子中,加州大学伯克利分校, 科学家发现 人们对如何的假设 细胞 修理 基因组 在 Cas9 之后 酶 剪 的DNA 错了。
这一发现揭示了为什么 CRISPR-Cas9 基因 编辑在几乎所有尝试的细胞中都非常有效,尽管并非在所有细胞中都取得了同样的成功。 它可以帮助研究人员提高细胞将新 DNA 插入基因组的效率——以取代有害的 突变 例如,使用正确的 DNA 序列——并通常调整 CRISPR-Cas9 编辑以获得所需的结果。
“如果你想治疗镰状细胞性贫血,你成功的机会与你用正确的基因替换突变的镰状细胞基因的效率密不可分,”加州大学伯克利分校的博士后研究员 Chris Richardson 说,他是一篇论文的第一作者。调查结果。 “如果你从一个病人身上收获了 10 万个细胞并且你有 30% 的插入率,那还不如你有 40% 到 XNUMX% 的插入率。 能够操纵这些细胞来增加这个过程的频率,称为 同源定向修复,令人兴奋。”
“基因编辑是超级强大的,有很多希望,但到目前为止,还有很多反复试验。 它在人类细胞中的工作方式一直是一个有很多假设的黑匣子,”主要作者、加州大学伯克利分校分子和细胞生物学兼职教授雅各布·科恩说。 “我们终于开始了解正在发生的事情。”
玉米、理查森和他们的同事将 发表他们的发现 在该杂志的 XNUMX 月刊中 “自然遗传学,将于 27 月 XNUMX 日在线提供。
直到最近,玉米还是创新中心的生物医学科学总监。 基因组学 Institute,加州大学伯克利分校和加州大学旧金山分校之间的联合 CRISPR 研究项目。 今年秋天,他将加入瑞士苏黎世的 ETH 学院。
CRISPR 依赖于 DNA 修复
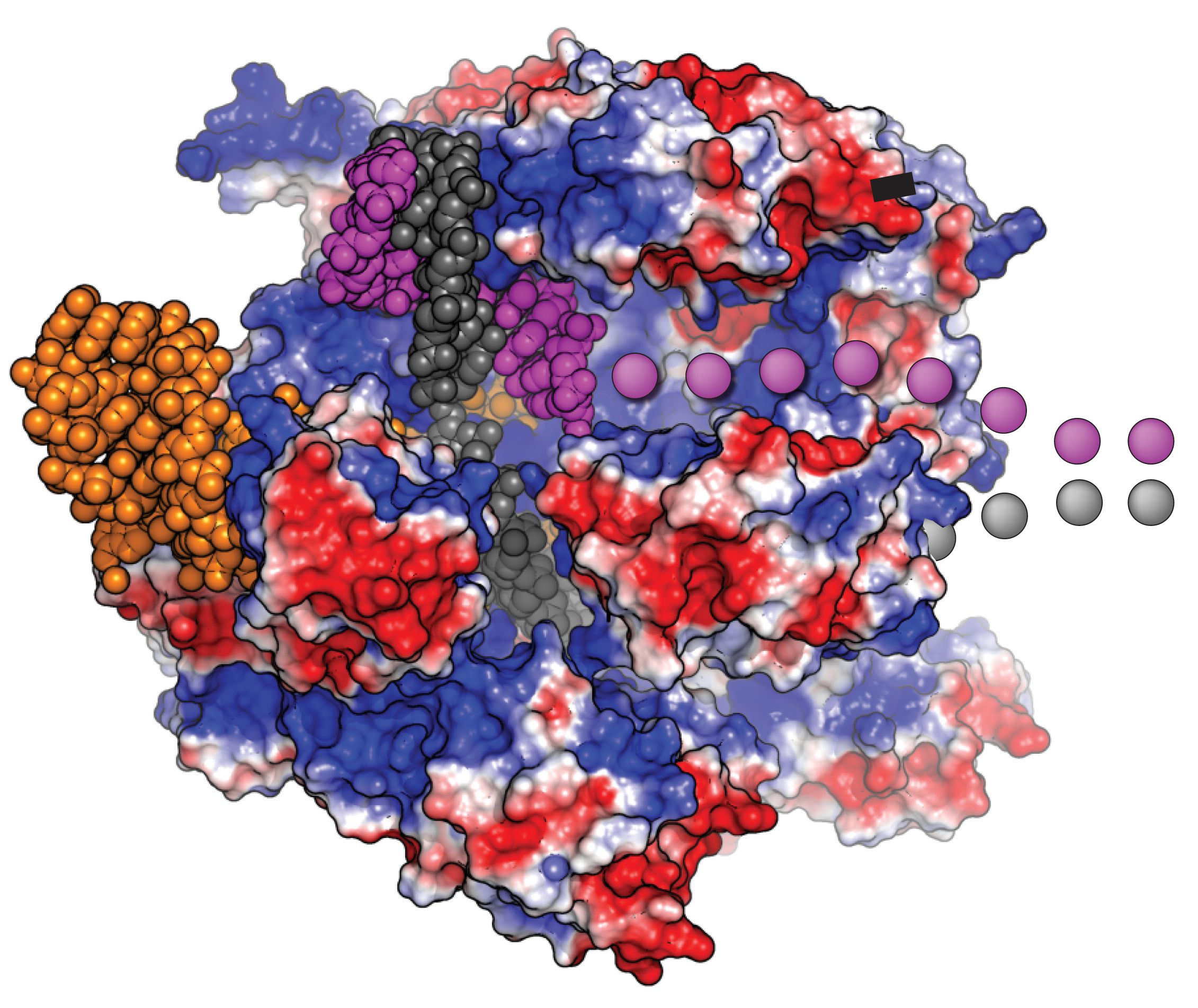
CRISPR-Cas9 是革命性的,因为它精确定位基因组中数十亿的特定 DNA 序列并切割 双链 脱氧核糖核酸分子。 但在那之后,由细胞来修复损伤。
修复可以通过两种方式进行。 酶可以将悬垂的末端重新缝合在一起,这通常会导致一个或多个 基础 被添加或删除,破坏基因的功能。 或者,其他酶可以用与切割上游和下游 DNA 序列匹配的单链 DNA 修补断裂。 一种 补充 DNA链的产生是为了完成双链修复。
前者称为 非同源端接,似乎是 CRISPR 切割后最常见的结果。 后者是同源定向修复,在某些类型的细胞中比其他类型的细胞发生得更频繁,并且需要存在可用于修补断裂的 DNA 片段。 研究人员通常会提供一段单链 DNA,并希望细胞用它来用新的序列替换错误的序列。
然而,这两个过程都有些神秘,没有人知道为什么有些细胞很容易在 DNA 中修补,而另一些则很少这样做。
“将 CRISPR-Cas9 用于医学或合成生物学应用的热情很高,但没有人真正知道将其放入细胞后会发生什么,”理查森说。 “它会产生这些断裂,你依靠细胞来修复它们。 但人们并不真正了解这个过程是如何运作的。”
为了找出哪些 DNA 修复酶对 CRISPR 切割后的同源定向修复至关重要,Richardson 和 Corn 采用了一种称为 CRISPR干扰 (CRISPRi) 一次敲除 2,000 多个已知或怀疑参与 DNA 修复的基因,这是一种对健康细胞至关重要的功能。
令人惊讶的是,许多被证明很重要的基因——当它们被沉默时同源定向修复急剧下降——参与了一个重要的修复系统,而这个系统被认为不参与 CRISPR 修复。
范可尼贫血
该途径涉及 21 个独立的 蛋白质 并且被称为范可尼贫血途径,因为如果这些蛋白质的任何基因受损,人们就会患上范可尼贫血症,这是一种罕见但严重的遗传性疾病,骨髓不能制造足够的新血细胞。 它与出生缺陷和高风险有关 癌症,包括 10% 的机会在儿童时期患上白血病。 很少有患者能活到 30 岁以上。
该途径已为人们所知和研究了数十年,但人们普遍认为它可以修复一种特定类型的 DNA 损伤:DNA 链间交联,其中 核苷酸 在一条 DNA 链上与相邻链上的核苷酸紧密结合,干扰 DNA 复制并经常杀死细胞。 Corn指出,1980年代的研究人员报告了同源定向修复与范可尼贫血途径之间的联系,但它被忽视或误解了。
“根据我们的工作,我们认为 Fanconi 贫血通路在修复其他类型的病变方面也发挥着重要作用,但最好将其理解为修复的通路 双链断裂,”理查森说。 “在 Cas9 编辑之后,如果你想插入新的 DNA,就需要 Fanconi 贫血通路。”
然而,范可尼贫血通路在修复 CRISPR 中断方面的重要性使一些计划用于该疾病本身的 CRISPR 治疗产生了怀疑。 如果没有活跃的范可尼贫血通路,细胞可能无法在 Cas9 切割后用正常基因替换其突变基因。
事实上,范可尼贫血通路的活性水平可能会影响 CRISPR 在特定细胞中插入 DNA 的效率。 研究人员得出结论,虽然末端连接是双链断裂后的默认修复机制,但范可尼贫血通路与之竞争,更高的活性导致更多的同源定向修复和更少的末端连接。
癌症治疗
虽然这些发现有助于科学家更好地了解人类细胞中的 DNA 修复机制,但它们也可以帮助研究人员开发针对癌细胞中 DNA 修复的抗癌疗法。 由于现在似乎还有其他因素参与了双链断裂的修复,因此这项研究扩展了可能被错误调节以破坏癌细胞中的 DNA 修复并使它们更容易死亡的蛋白质列表。
理查森还发现,该途径中的 21 种蛋白质之一 FANCD2 始终位于 CRISPR-Cas9 产生的双链断裂位点,表明它在调节新 DNA 插入基因组中起着重要作用。切割现场。 可以调整 FANCD2 以提高细胞通过同源定向修复插入 DNA 的频率。
“此外,由于 FANCD2 定位于 Cas9 断裂的位置,您可以使用 FANCD2 来绘制 Cas9 在任何细胞类型中切割的位置,”理查森说。 “如果您编辑一组细胞,并且想知道打开和 不中 切割是,你只需绘制基因组中发现 FANCD2 的位置,就可以找到切割。”
“整个范可尼贫血通路影响末端连接和同源定向修复之间的平衡; 它就像一个交通警察,”康说。 “因此,患者的基因型会影响您进行基因编辑的方式。”
加州大学伯克利分校的其他作者是 Katelynn Kazane、Sharon Feng、Elena Zelin、Nicholas Bray、Axel Schäfer 和 Stephen Floor,他现在在加州大学旧金山分校。 这项工作得到了李嘉诚基金会、传统医学研究所和范可尼贫血研究基金会的资助。