noticias
La nueva comprensión de la herramienta CRISPR-Cas9 podría mejorar la edición del genoma
Una nueva comprensión de la herramienta CRISPR-Cas9 podría mejorar la edición del genoma
Noticias de Berkeley | Robert Sanders | 30 de julio de 2020

En tan solo ocho años, CRISPR-Cas9 se ha convertido en el favorito genoma, editor de investigación básica y terapias de genes. Pero CRISPR-Cas9 también ha engendrado otros potencialmente poderosos ADN herramientas de manipulación que podrían ayudar a corregir la genética mutaciones responsable de enfermedades hereditarias.
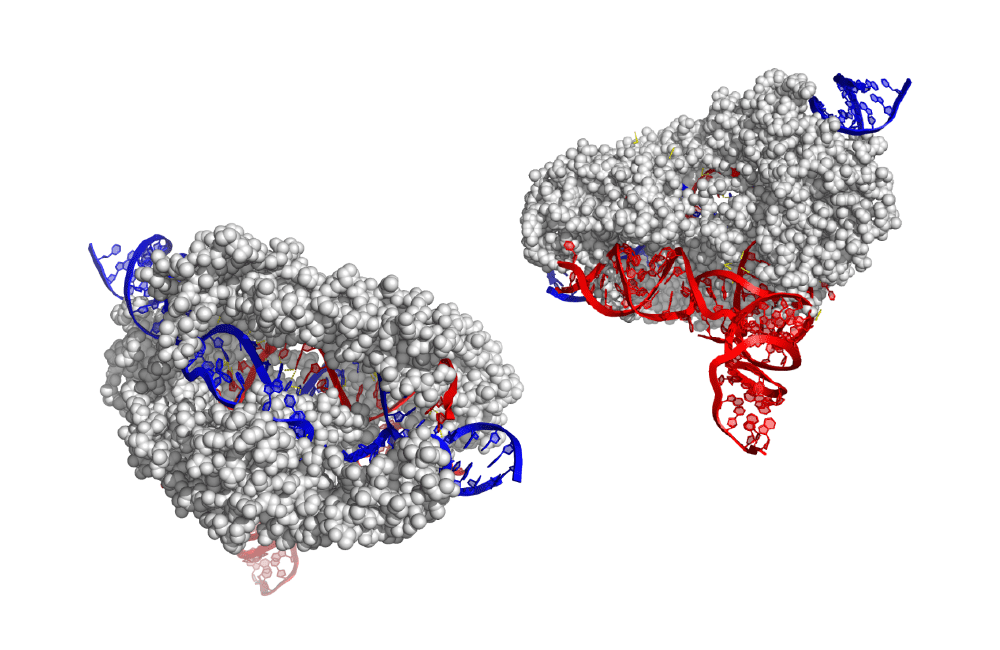
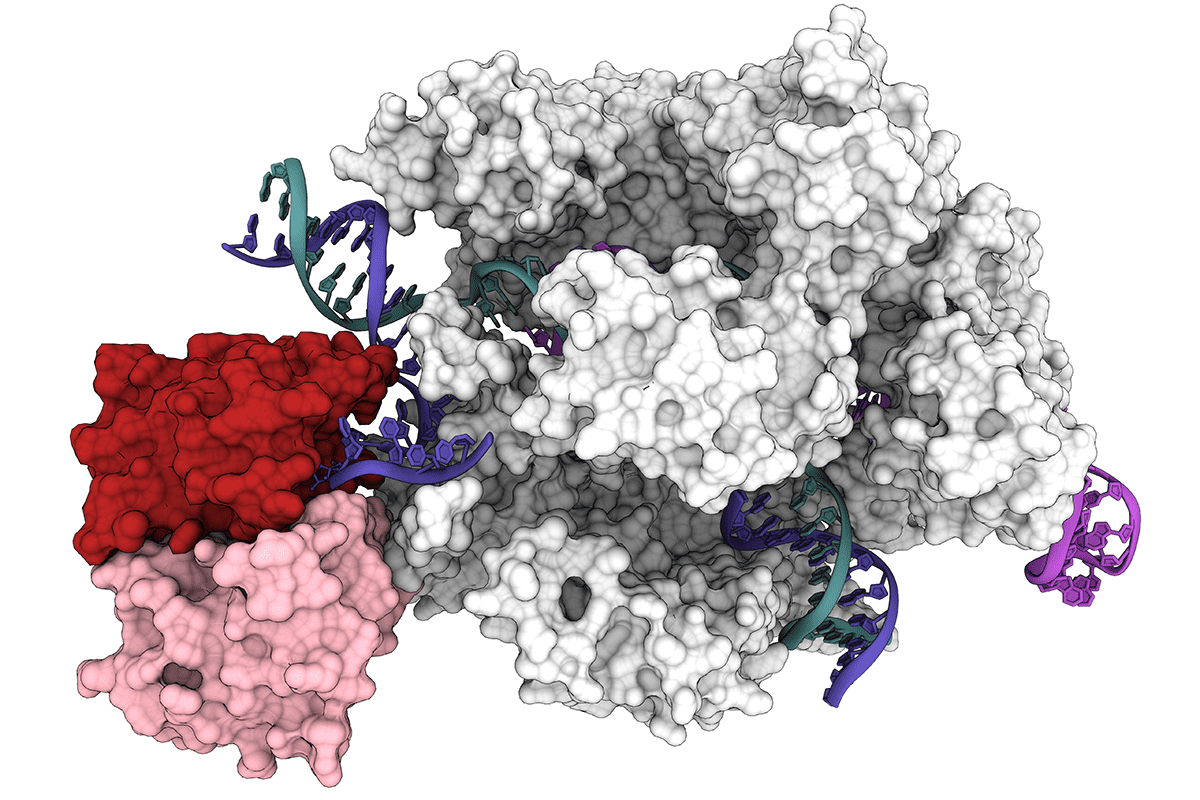
Los científicos de la Universidad de California, Berkeley, han obtenido la primera estructura 3D de una de las herramientas más prometedoras: editores de bases, que se unen al ADN y, en lugar de cortar, reemplazan con precisión uno nucleótido con otro.
Creado por primera vez hace cuatro años, bases ya se están utilizando editores para intentar corregir mutaciones de un solo nucleótido en el genoma humano. Los editores de base ahora disponibles podrían abordar aproximadamente el 60% de todas las enfermedades genéticas conocidas, potencialmente más de 15,000 trastornos hereditarios, causados por una mutación en un solo nucleótido.
La estructura 3D detallada, informada en la edición del 31 de julio de la revista. Ciencia:, proporciona una hoja de ruta para ajustar los editores básicos para hacerlos más versátiles y controlables para su uso en pacientes.
“Pudimos observar por primera vez a un editor de base en acción”, dijo el becario postdoctoral de UC Berkeley, Gavin Knott. "Ahora podemos entender no solo cuándo funciona y cuándo no, sino también diseñar la próxima generación de editores básicos para hacerlos aún mejores y más apropiados desde el punto de vista clínico".
Un editor base es un tipo de fusión Cas9 proteína que emplea un Cas9 parcialmente desactivado: sus tijeras de corte están desactivadas para que corte solo una hebra de ADN - y un enzima que, por ejemplo, activa o silencia un gen, o modifica áreas adyacentes de ADN. Debido a que el nuevo estudio informa la primera estructura de una proteína de fusión Cas9, podría ayudar a guiar la invención de muchas otras herramientas de edición del genoma basadas en Cas9.
"De hecho, vemos por primera vez que los editores base se comportan como dos módulos independientes: tienes el módulo Cas9 que te da especificidad, y luego tienes un módulo catalítico que te proporciona la actividad", dijo Audrone Lapinaite, ex UC Berkeley becario postdoctoral que ahora es profesor asistente en la Universidad Estatal de Arizona en Tempe. "Las estructuras que obtuvimos de este editor de base unidas a su objetivo realmente nos dan una forma de pensar acerca de las proteínas de fusión Cas9, en general, dándonos ideas sobre qué región de Cas9 es más beneficiosa para fusionar otras proteínas".
Lapinaite y Knott, que recientemente aceptaron un puesto como investigador en la Universidad de Monash en Australia, son los primeros coautores del artículo.
"Esta estructura nos ayuda a comprender a los editores de base a un nivel mucho más profundo", dijo la autora principal Jennifer Doudna, profesora de Molecular y Celular Biología y fundadora y presidenta de la junta de Innovative Genómica Instituto. "Ahora que podemos ver con qué estamos trabajando, podemos desarrollar estrategias informadas para mejorar el sistema".
Editar una base a la vez
En 2012, los investigadores mostraron por primera vez cómo rediseñar un bacteriano enzima, Cas9, y conviértala en una herramienta de edición del genoma en todo tipo de células, desde bacterianas hasta humanas. CRISPR-Cas9, creación de Doudna y su colega francesa, Emmanuelle Charpentier, ha transformado la investigación biológica y ha llevado la terapia génica a la clínica por primera vez en décadas.
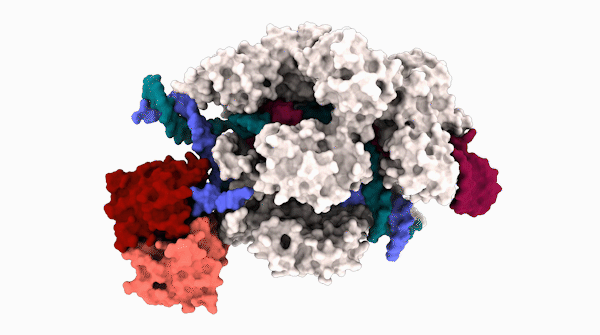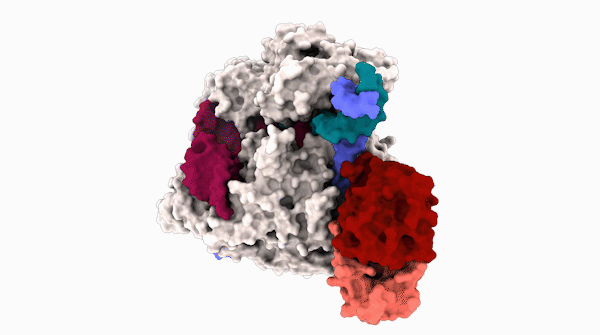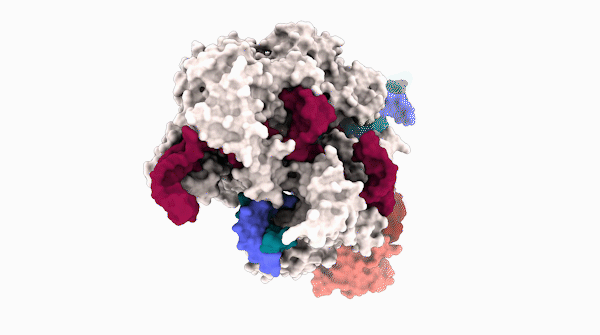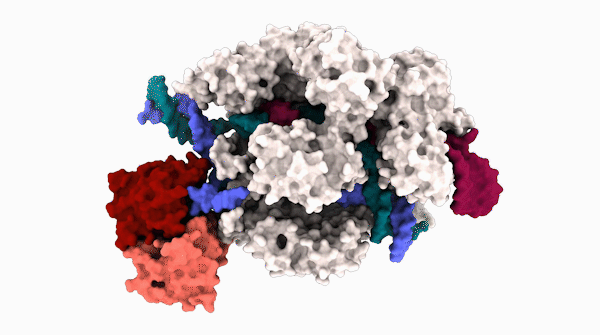
Los científicos rápidamente eligieron Cas9 para producir una gran cantidad de otras herramientas. Básicamente una mezcla de proteínas y moléculas de ARN, Cas9 apunta con precisión a un tramo específico de ADN y luego lo corta con precisión, como un par de tijeras. Sin embargo, la función de tijeras puede romperse, lo que permite que Cas9 apunte y se una al ADN sin cortar. De esta manera, Cas9 puede transportar diferentes enzimas a regiones específicas de ADN, lo que permite que las enzimas manipulen genes.
En 2016, David Liu de la Universidad de Harvard y el Instituto Broad del Instituto de Tecnología de Massachusetts y Harvard combinaron un Cas9 con otra proteína bacteriana para permitir el reemplazo quirúrgicamente preciso de un nucleótido con otro: el editor de primera base.
Si bien el editor de base de adenina inicial era lento, la versión más reciente, llamada ABE8e, es increíblemente rápida: completa casi el 100% de las ediciones de base previstas en 15 minutos. Sin embargo, ABE8e puede ser más propenso a editar fragmentos de ADN no deseados en un tubo de ensayo, creando potencialmente lo que se conoce como fuera del objetivo efectos.
La estructura recién revelada se obtuvo con una técnica de imagen de alta potencia llamada microscopía crioelectrónica (cryoEM). Los ensayos de actividad mostraron por qué ABE8e es propenso a crear más ediciones fuera del objetivo: la proteína desaminasa fusionada con Cas9 siempre está activa. A medida que Cas9 salta alrededor del núcleo, se une y libera cientos o miles de segmentos de ADN antes de encontrar su objetivo previsto. La desaminasa adjunta, como un cañón suelto, no espera una combinación perfecta y, a menudo, edita una base antes de que Cas9 se detenga en su objetivo final.
Saber cómo están vinculados el dominio efector y Cas9 puede conducir a un rediseño que active la enzima solo cuando Cas9 haya encontrado su objetivo.
“Si realmente desea diseñar una proteína de fusión verdaderamente específica, debe encontrar una manera de hacer que el dominio catalítico sea más parte de Cas9, de modo que sienta cuando Cas9 está en el objetivo correcto y solo entonces se activa, en lugar de ser activo todo el tiempo ”, dijo Lapinaite.
La estructura de ABE8e también señala dos cambios específicos en la proteína desaminasa que hacen que funcione más rápido que la versión anterior del editor base, ABE7.10. Esas dos mutaciones puntuales permiten que la proteína se adhiera al ADN con más fuerza y reemplace de manera más eficiente A con G.
“Como biólogo estructural, realmente quiero mirar una molécula y pensar en formas de mejorarla racionalmente. Esta estructura y la bioquímica que la acompaña realmente nos dan ese poder ”, agregó Knott. "Ahora podemos hacer predicciones racionales sobre cómo se comportará este sistema en una célula, porque podemos verlo y predecir cómo se romperá o predecir formas de mejorarlo".
"Si bien los editores de base ahora se utilizan ampliamente para introducir cambios precisos en organismos que van desde bacterias a plantas y primates, nadie ha observado previamente la estructura molecular tridimensional de un editor de base", dijo Liu, quien también es un Instituto Médico Howard Hughes. investigador. "Este proyecto de colaboración revela la hermosa estructura molecular de un editor de base altamente activo y de última generación, ABE8e, atrapado en el acto de activar un sitio de ADN objetivo".
Además de Lapinaite, Knott, Doudna y Liu, otros coautores del artículo son Cody Palumbo y Peter Beal de UC Davis, Enrique Lin Shiao de UC Berkeley & the IGI, y Michelle Richter y Kevin Zhao del Broad Institute, una colaboración entre Harvard y el Instituto de Tecnología de Massachusetts.
INFORMACIÓN RELACIONADA
- Captura de ADN mediante un editor de base de adenina guiado por CRISPR-Cas9 (Ciencia:)
- Sitio web del laboratorio Doudna
Contactos para los medios de comunicación
Audrey Lapinaite: audrone.lapinaite@asu.edu
Gavin Knott: gavin.knott@berkeley.edu, gavin.knott@monash.edu
Andy Murdock: andymurdock@berkeley.edu


