
noticias
Descubriendo un paso oculto en CRISPR "Cortar y pegar"
IGI | Maya Kostman | 27 de julio de 2018
La reparación del ADN después del corte de CRISPR no es en absoluto lo que la gente pensaba
Noticias de Berkeley | Robert Sanders | 30 de julio de 2018
A pesar de las grandes esperanzas y la gran inversión en CRISPR-Cas9 edición de genes, los científicos aún tienen mucho que aprender sobre cómo funciona en humanos.
En el último ejemplo, la Universidad de California, Berkeley, los científicos encontraron que las suposiciones de la gente sobre cómo células reparar el genoma, después del Cas9 enzima recortes ADN estan equivocados.
El descubrimiento da una idea de por qué CRISPR-Cas9 gen la edición funciona notablemente bien en casi todos los intentos de celda, aunque no con el mismo éxito en todas las celdas. Y podría ayudar a los investigadores a aumentar la eficiencia con la que las células insertan nuevo ADN en el genoma, para reemplazar un dañino. crianza de organismos con mutación deseada con la secuencia de ADN correcta, por ejemplo, y generalmente modifique la edición CRISPR-Cas9 para obtener el resultado deseado.
"Si desea tratar la anemia de células falciformes, sus posibilidades de éxito están inextricablemente ligadas a la eficiencia con la que puede reemplazar el gen de células falciformes mutado por el correcto", dijo el becario postdoctoral de UC Berkeley Chris Richardson, primer autor de un artículo que describe los resultados. “Si recolecta un millón de células de un paciente y tiene una tasa de inserción del 10 por ciento, eso no es tan bueno como si tuviera entre un 30 y un 40 por ciento. Ser capaz de manipular esas células para aumentar la frecuencia de este proceso, llamado reparación dirigida por homología, es emocionante."
“La edición de genes es superpoderosa, prometedora pero, hasta ahora, mucha prueba y error. La forma en que funciona en las células humanas ha sido una caja negra con muchas suposiciones ”, dijo el autor principal Jacob Corn, profesor adjunto de biología molecular y celular de UC Berkeley. "Finalmente estamos empezando a tener una idea de lo que está pasando".
Corn, Richardson y sus colegas publicar sus hallazgos en el número de agosto de la revista Nature Genetics, que estará disponible en línea el 27 de julio.
Corn fue hasta hace poco el director científico de biomedicina en el Innovative Genómica Institute, un programa de investigación CRISPR conjunto entre UC Berkeley y UC San Francisco. Este otoño, se unirá a la facultad de ETH en Zurich, Suiza.
CRISPR se basa en la reparación del ADN
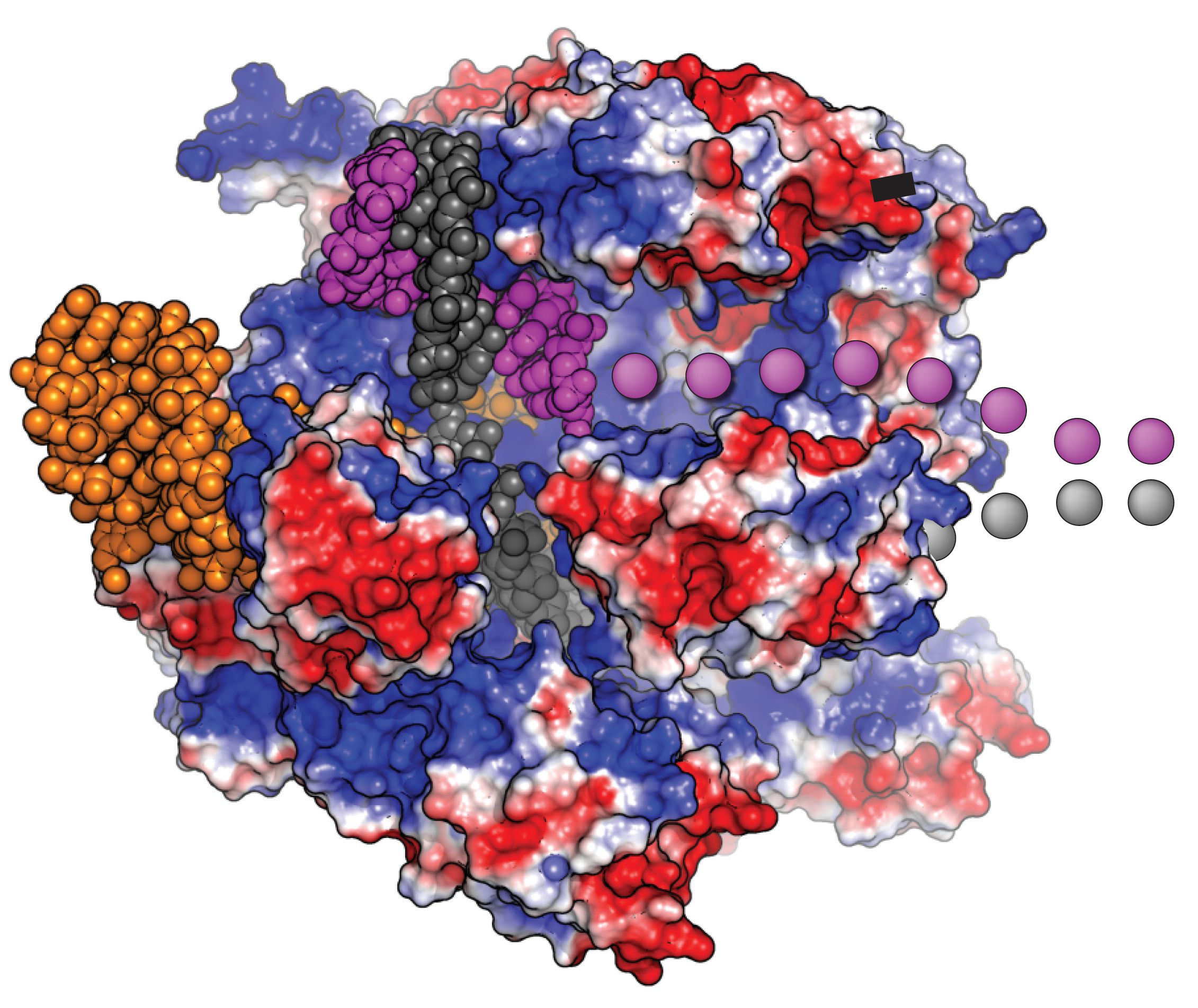
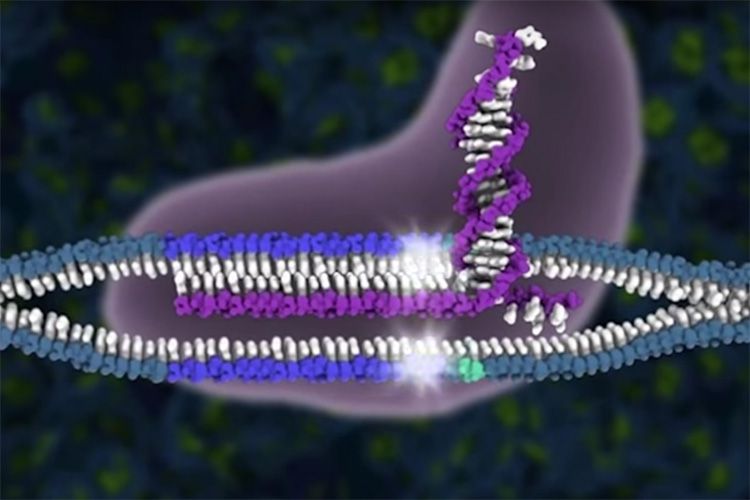
CRISPR-Cas9 es revolucionario debido a la precisión con la que se ubica en una secuencia de ADN específica de miles de millones en el genoma y escinde el doble hebra Molécula de ADN. Pero después de eso, depende de la célula reparar el daño.
La reparación puede ocurrir de dos formas. Las enzimas pueden volver a unir los extremos colgantes, lo que a menudo da como resultado uno o más bases ser agregado o eliminado, interrumpiendo la función del gen. Alternativamente, otras enzimas pueden parchear la ruptura con una sola hebra de ADN que coincida con la secuencia de ADN corriente arriba y corriente abajo del corte. A complementario La hebra de ADN se crea para completar la reparación de la doble hebra.
El primero, llamado unión final no homóloga, parece ser el resultado más común después del corte CRISPR. La última, la reparación dirigida por homología, ocurre con más frecuencia en algunos tipos de células que en otras, y requiere la presencia de un fragmento de ADN que pueda usarse para parchear la ruptura. Los investigadores a menudo proporcionan un fragmento de ADN de una sola hebra y esperan que la célula lo utilice para reemplazar la secuencia defectuosa por la nueva.
Sin embargo, ambos procesos son un poco misteriosos y nadie sabe por qué algunas células se insertan fácilmente en el ADN mientras que otras lo hacen con poca frecuencia.
“El entusiasmo por usar CRISPR-Cas9 para aplicaciones médicas o de biología sintética es grandioso, pero nadie sabe realmente qué sucede después de colocarlo en las células”, dijo Richardson. “Va y crea estas roturas y cuentas con las células para arreglarlas. Pero la gente realmente no entiende cómo funciona ese proceso ".
Para averiguar qué enzimas de reparación del ADN son críticas para la reparación dirigida por homología después del corte CRISPR, Richardson y Corn emplearon una técnica llamada Interferencia CRISPR (CRISPRi) para eliminar, uno a la vez, más de 2,000 genes que se sabe o se sospecha que están involucrados en la reparación del ADN, una función fundamental para una célula sana.
Sorprendentemente, muchos de los genes que demostraron ser importantes (la reparación dirigida por homología disminuyó drásticamente cuando se silenciaron) estaban involucrados en un sistema de reparación importante que no se cree que esté involucrado en la reparación CRISPR.
Anemia de Fanconi
El camino involucra 21 separados proteínas y se denomina vía de la anemia de Fanconi porque, si se daña alguno de los genes de estas proteínas, las personas desarrollan anemia de Fanconi, una enfermedad hereditaria rara pero grave en la que la médula ósea no puede producir suficientes células sanguíneas nuevas. Está asociado con defectos de nacimiento y un alto riesgo de células cancerosas, incluida una probabilidad del 10 por ciento de desarrollar leucemia en la niñez. Pocos pacientes viven más allá de los 30 años.
La vía se ha conocido y estudiado durante décadas, pero se entendió en gran medida que repara un tipo específico de daño en el ADN: los enlaces cruzados entre cadenas de ADN, donde un nucleótido en una hebra de ADN se une estrechamente con un nucleótido de la hebra adyacente, lo que interfiere con la replicación del ADN y, a menudo, mata la célula. Los investigadores en la década de 1980 habían informado de una conexión entre la reparación dirigida por homología y la vía de la anemia de Fanconi, pero había sido ignorada o malinterpretada, anotó Corn.
“Basándonos en nuestro trabajo, creemos que la vía de la anemia de Fanconi también juega un papel importante en la reparación de otros tipos de lesiones, pero se entiende mejor como la vía que repara roturas de doble hebra”, Dijo Richardson. "Después de la edición de Cas9, se requiere la vía de anemia de Fanconi si desea insertar ADN nuevo".
Sin embargo, la importancia de la vía de la anemia de Fanconi en la reparación de roturas CRISPR pone en duda algunos tratamientos CRISPR planificados para la enfermedad en sí. Sin una vía de anemia de Fanconi activa, es posible que las células no puedan reemplazar sus genes mutados con genes normales después de que Cas9 haga un corte.
De hecho, el nivel de actividad de la vía de la anemia de Fanconi puede afectar la eficiencia con la que CRISPR puede insertar ADN en una célula específica. Los investigadores concluyeron que, si bien la unión de los extremos es el mecanismo de reparación predeterminado después de una rotura de doble hebra, la vía de la anemia de Fanconi compite con ella, y que una mayor actividad da como resultado una reparación más dirigida por homología y una menor unión de los extremos.
Tratamientos contra el cáncer
Si bien los hallazgos ayudan a los científicos a comprender mejor los mecanismos de reparación del ADN en las células humanas, también podrían ayudar a los investigadores a desarrollar terapias contra el cáncer que se dirijan a la reparación del ADN en las células cancerosas. Debido a que ahora parecen estar involucrados otros factores en la reparación de roturas de doble hebra, esta investigación amplía la lista de proteínas que podrían estar mal reguladas para estropear la reparación del ADN en las células cancerosas y hacerlas más susceptibles a la muerte.
Richardson también descubrió que una de las 21 proteínas en la vía, FANCD2, siempre se aloja en el sitio de la ruptura de la doble hebra creada por CRISPR-Cas9, lo que indica que desempeña un papel importante en la regulación de la inserción de nuevo ADN en el genoma en el sitio del corte. FANCD2 podría modificarse para aumentar la frecuencia con la que una célula inserta ADN a través de la reparación dirigida por homología.
“Además, dado que FANCD2 se localiza en el sitio de las roturas de Cas9, puede usar FANCD2 para mapear dónde está cortando Cas9 en cualquier tipo de celda”, dijo Richardson. "Si edita una población de celdas y desea saber dónde están fuera del objetivo "
“Toda la vía de la anemia de Fanconi afecta el equilibrio entre la unión de los extremos y la reparación dirigida por homología; actúa como un policía de tráfico ”, dijo Corn. "Por lo tanto, el genotipo de un paciente afectará la forma en que se realiza la edición de genes".
Otros autores de UC Berkeley son Katelynn Kazane, Sharon Feng, Elena Zelin, Nicholas Bray, Axel Schäfer y Stephen Floor, quien ahora está en UCSF. El trabajo fue apoyado por subvenciones de la Fundación Li Ka Shing, el Instituto de Investigación Médica Heritage y la Fundación de Investigación de la Anemia Fanconi.